Las vesículas extracelulares de ratones deficientes en CD38 tratados con pristano expresan una firma de proteínas antiinflamatorias procedente de neutrófilos, que refleja la menor gravedad del lupus inducido en estos ratones.
Paula Carrillo-Rodríguez, José-Ángel Robles-Guirado, Adrián Cruz-Palomares, Miguel Ángel Palacios-Pedrero, Elena González-Paredes, Alex Más-Ciurana, Carolina Franco- Herrera, Paloma A Ruiz-de-Castroviejo-Teba, Antonio Lario, Victoria Longobardo, Laura Montosa-Hidalgo, Maria Pérez Sánchez-Cañete, María-Mercedes Corzo-Corbera, Sandra Redondo-Sánchez, Ana-Belén Jodar, Francisco J Blanco, Esther C Zumaquero, Ramón Merino, Jaime Sancho and Mercedes Zubiaur.
Front. Immunol., 24 October 2022
RESUMEN
Las vesículas extracelulares (EV) están presentes en todos los fluidos corporales. Liberadas por células, su composición molecular refleja la de su célula de origen y/o la situación patológica del tejido donde se liberan, siendo muy útiles en la búsqueda de biomarcadores propios de una enfermedad concreta. En ratones deficientes en CD38, la inyección intraperitoneal de pristano induce una enfermedad autoinmune similar al lupus humano, siendo más leve que la inducida en ratones WT. El objetivo de este estudio fue analizar en las EV liberadas por las células de exudados peritoneales en el modelo experimental de lupus inducido por pristano, la composición proteica, la abundancia de las proteínas identificadas y la integración de las mismas en redes funcionales. El objetivo final ha sido el identificar biomarcadores predictivos o de diagnóstico que podrían discriminar el proceso autoinmune que se desarrolla en el lupus de las reacciones inflamatorias y/o los procesos fisiológicos normales. Así, gracias a un extenso análisis proteómico y un potente software de bioinformática, se identificaron distintos subtipos de EV en los exudados peritoneales de los ratones tratados con pristano: 1) EV de pequeño tamaño enriquecidas en las tetraspaninas CD63 y CD9, que probablemente sean de origen exosomal; 2) EV de pequeño tamaño enriquecidas en CD47 y CD9, que también están enriquecidos en proteínas asociadas a la membrana plasmática, y que son de origen ectosomal; 3) EV pequeñas enriquecidas en queratinas, proteínas de la matriz extracelular, proteínas del complemento/coagulación, proteínas que intervienen en la formación de coágulos de fibrina y proteínas inhibidoras de la actividad endopetidasa. Este enriquecimiento en estas proteínas es clave en este estudio, ya que parecen reflejar la transición mesotelio-mesenquima que ocurre en el peritoneo como consecuencia de la inflamación inducida por pristano. Estas proteínas se detectan en la superficie de las EV y otras nanopartículas formando una estructura denominada corona de proteínas, que dotan a estas nanoestructuras de importantes capacidades funcionales; 4) Partículas de lipoproteínas enriquecidas con HDL. El análisis proteómico cuantitativo nos permitió identificar una firma de proteínas antiinflamatoria procedente de neutrófilos. Una de las proteínas de esa firma es la anexina A1, que es una proteína clave en el proceso de resolución de la inflamación. Esta proteína, y las otras que forman parte de la firma antiinflamatoria, es más abundante en las EV procedentes de ratones deficientes en CD38 que en los ratones WT. También observamos diferencias cuantitativas en las proteínas de la matriz extracelular y de otras proteínas que forman la corona de proteínas que tapizan las EV de exudados peritoneales. Estas diferencias reflejan la diferente respuesta inflamatoria a la inyección de pristano provocada en ratones deficiente en CD38 vs ratones WT. En resumen, nuestros resultados demuestran el poder de un enfoque holístico, basado en datos ómicos, para transformar la inherente heterogeneidad de las proteínas presentes en las EV procedentes de exudados peritoneales de ratones tratados con pristano en información valiosa sobre la proporción relativa de los diferentes tipos de EV que se detectan en una muestra determinada y que sirven para identificar biomarcadores de proteínas específicos para cada uno de los subtipos de EV y su función. En particular, en este estudio hemos identificado aquellas proteínas que definen EV involucradas en la fase de resolución de la inflamación crónica. Estos hallazgos pueden ser útiles, en un enfoque de medicina traslacional o de biopsia líquida, para la identificación de biomarcadores no invasivos que sean útiles para el diagnóstico y seguimiento de pacientes con enfermedades autoinmunes, como el lupus eritematoso sistémico.
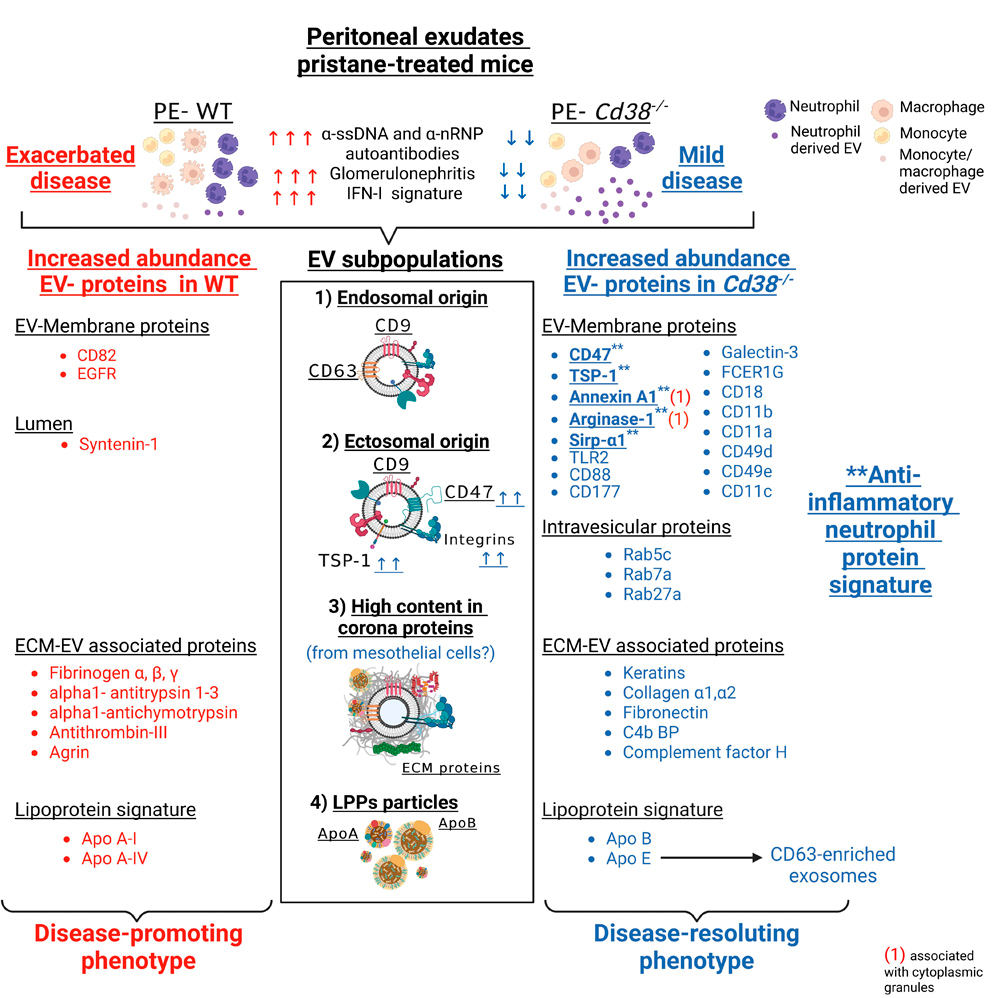
Fig: Representación esquemática de los principales hallazgos de este estudio. Las proteínas se asignaron a los diferentes tipos de EV y partículas de lipoproteínas presentes en los exudados peritoneales de ratones WT tratados con pristano (resaltados en rojo, a la izquierda) frente a ratones deficientes en CD38 (resaltados en azul, a la derecha), como lo sugieren los análisis de comparación proteómica cuantitativa. Solo se muestra una fracción de las proteínas, que son parte de la firma antiinflamatoria de proteínas procedente de neutrófilos .
Sec. Inflammation
https://doi.org/10.3389/fimmu.2022.1013236
